结核病(TB)仍是全球头号传染病杀手。结核分枝杆菌(Mtb)感染皮肤引起的皮肤结核病(CTB)严重威胁公共卫生安全和人民群众生命健康。皮肤结核目前缺乏针对性的治疗方案,临床上沿用肺结核治疗的方案进行联合用药治疗,尚无确定和经过验证的疗程方案可用,亟待开发更有效的治疗方法。
激光疗法是一类利用激光高单色性、高方向性、高亮度、高相干性等特性等特殊性能治疗疾病的方法。激光照射生物组织时可产生光效应、热效应,压力效应和电磁场效应等,从而在生物医学领域,尤其是皮肤美容和皮肤疾病治疗方面得到广泛应用。光热疗法(PTT)是一种新兴的疾病治疗手段,利用具有较高光热转换效率的材料,在近红外(NIR)光照射下产生足够的热量以杀伤肿瘤细胞或者病原体。PTT具有高选择性、低侵入性以及无系统性副作用等,从而有望用于结核病的治疗技术开发。刘蓓/褚洪迁/朱传智等前期报道了纳米材料介导的光热/光动力联合作用实现有效抗菌的潜在抗结核策略(Acta Materia Medica, 2023),廖玉辉/唐本忠/王东等进一步报道了纳米材料介导的PTT能诱导高热以有效杀伤肺部肉芽肿内结核分枝杆菌的抗结核策略(Nat Nanotechnol, 2024; Adv Mater, 2024)。但能否基于功能纳米材料开发光热疗法用于皮肤结核病的治疗,以及能否通过光热疗法激活宿主抗结核免疫功能以更有效清除Mtb感染仍是一个挑战。
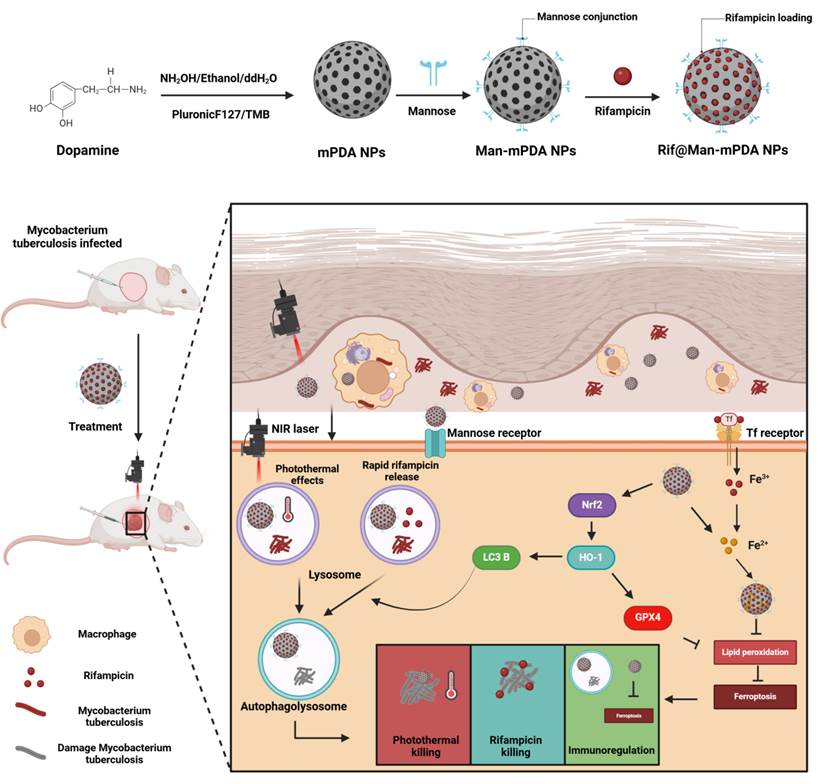
2024年9月,皮江/杨芬博士团队与美国伊利诺伊大学医学院Ling Shen教授团队联合在Materials Today Bio(中科院一区,影响因子8.7)发表论文Photothermal and Host Immune Activated Therapy of Cutaneous Tuberculosis using Macrophage Targeted Mesoporous Polydopamine Nanoparticles,报道了基于聚多巴胺-光热疗法协同靶向药物杀伤和宿主细胞抗结核免疫功能增强的抗皮肤结核新策略(以下简称:Rif@Man-mPDA NPs介导的PTT)。本研究构建了甘露糖修饰的介孔聚多巴胺纳米系统(Man-mPDA NPs),作为靶向巨噬细胞药物载体的同时,也作为光热剂开发针对Mtb感染巨噬细胞的光热治疗策略(PTT),Rif@Man-mPDA NPs介导的PTT疗法能结合巨噬细胞靶向的抗结核药物杀伤、以及光热介导的高热和宿主细胞抗结核免疫功能增强,以更有效抑制Mtb感染,为开发更有效的皮肤结核治疗技术提供新的思路和依据。
医学技术学院硕士研究生范书豪为第一作者,医学技术学院教师赵黛娜博士和博士研究生王家俊为共同第一作者,皮江博士和杨芬博士为共同通讯作者。该研究得到国家自然科学基金(82272348, 82270013,82300016)、广东省自然科学基金(2023A1515030195, 2022A1515011223, 2023A1515140072, 2022A1515010525,2023A1515110502)、松山湖医工联合项目(4SG22309P)等项目的大力支持。
(图文/范书豪,审核/皮江,终审/张华)

